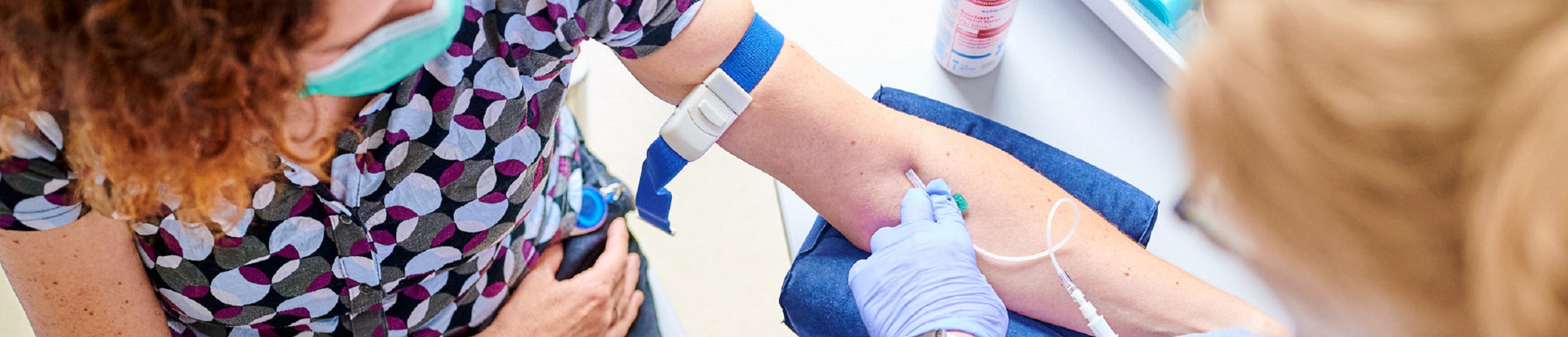
Probanden

Auf diesen Seiten finden Sie Informationen zu klinischen Studien und deren Ablauf und wie Sie an klinischen Studien als Proband teilnehmen können.
Die klinische Forschung und der medizinische Fortschritt sind ohne freiwillige Probanden, die an klinischen Studien teilnehmen, nicht möglich. Für den Fall, dass Sie gerne als Proband an einer Studie teilnehmen wollen, können Sie uns jederzeit direkt kontaktieren.
Ablauf einer klinischen Studie
Bevor ein Proband an einer Studie teilnimmt, findet zunächst ein Vorgespräch statt, in dem ausführlich über die Studie informiert wird. Nach ausreichender Bedenkzeit und schriftlicher Einwilligung des Probanden kann mittels einer körperlichen Untersuchung und ggf. weiterer Untersuchungen (z.B. einer Blutentnahme) beurteilt werden, ob der Proband an der jeweiligen Studie teilnehmen kann. Anschließend wird der Proband auf unsere Station zum Studienbeginn einbestellt. Hier wird typischerweise eine Venenverweilkanüle gelegt und eine Blutprobe entnommen. In einer pharmakologischen Studie erhält der Teilnehmer die erste Dosis des zu verabreichenden Medikaments. Hierbei handelt es sich entweder um die Versuchstherapie oder ein Vergleichsmedikament. Ggf. weiß weder der Arzt noch der Proband, wer in welche Gruppe gelost wurde (Doppelblind-Studie). Im weiteren Verlauf werden je nach Studie mehrere Blutentnahmen über die Venenverweilkanüle abgenommen und mehrere Medikamentendosen eingenommen. Dabei kann es erforderlich sein, dass der Proband nüchtern bleibt, um die Ergebnisse der Blutproben nicht zu verfälschen. Außerdem werden je nach Studie weitere Untersuchungen vorgenommen, z.B. Blutdruck, Puls, EKG und Temperatur. Dies kann sich je nach Studie über einige Stunden bis mehrere Tage erstrecken und einen Aufenthalt auf unserer Probandenstation über diese Zeit erfordern.
Darüber hinaus gibt es Studien, die ambulant durchgeführt werden. Dabei finden die Untersuchungen statt, ohne dass ein stationärer Aufenthalt über Nacht erforderlich ist.
Phasen Klinischer Studien
Um Erkrankungen besser behandeln zu können, müssen u. a. neue Medikamente entwickelt oder die Therapie mit vorhandenen Wirkstoffen verbessert werden. Neben Untersuchungen, die im Labor oder an Tiermodellen erfolgen, ist letztlich die Erprobung an Menschen entscheidend. Diese wird im Rahmen von so genannten klinischen Studien durchgeführt. Eine klinische Studie ist also die wissenschaftliche Testung von Arzneimitteln oder Medizingeräten an freiwilligen Patienten oder gesunden Probanden. Nur dadurch lässt sich nachweisen, ob das Arzneimittel/ Medizingerät sicher ist und eine positive Wirkung besitzt.
Bevor neue Wirkstoffe, neue Wirkstoffkombinationen oder neue Anwendungsmöglichkeiten für bekannte Wirkstoffe von den Behörden zugelassen und in die Praxis übernommen werden, müssen verschiedene Phasen klinischer Studien am Menschen durchlaufen werden. Studienteilnehmer spielen dabei eine wichtige Rolle.
Die Erstanwendung am Menschen (first in man / FIM) findet in der Phase I an einer kleinen Anzahl (10 – 50) gesunder, meist jüngerer Studienteilnehmer oder in Ausnahmefällen ausgewählter Patienten (z.B. bei Aids- oder Krebsmedikamenten) statt. Sie dient der Beurteilung der Sicherheit und Verträglichkeit sowie der Einschätzung von Nebenwirkungen. Außerdem werden die Aufnahme, Verteilung und Ausscheidung der Substanz bestimmt sowie erste Abschätzungen einer wirksamen Dosis vorgenommen
In der Phase II wird das Präparat zum ersten Mal an (hundert bis mehreren hundert) Patienten angewendet. Hierbei wird insbesondere die therapeutische Wirksamkeit und die Höhe der anzuwendenden Dosis sowie die auftretenden Nebenwirkungen untersucht.
Wurden die ersten beiden Phasen erfolgreich abgeschlossen wird das neue Medikament in der Phase III einer größeren Anzahl von Patienten (mehrere hundert bis tausend) verabreicht, und zwar in der endgültigen Dosierung und Verabreichungsform (z. B. als Tablette, Dragee oder Infusion). Das Ziel ist der Beweis oder die Bestätigung eines therapeutischen Nutzens. Dafür wird üblicherweise das neue Medikament mit den bisher verfügbaren Therapien verglichen oder ein Plazebo (= Scheinmedikament) als Vergleichspräparat eingesetzt.
Auf Basis der gesamten Studienergebnisse muss für die Zulassung durch die Behörden (Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM), Paul-Ehrlich-Institut (PEI) oder die europäische Zulassungsbehörde EMA) die Wirksamkeit und Verträglichkeit des Präparats nachgewiesen werden. Erst danach ist das Medikament auch außerhalb von Studien für jeden Patienten erhältlich.
Nach der Zulassung wird in der Phase IV überprüft, ob in der täglichen Praxis bei Anwendung bei einer großen Zahl von Patienten die langfristige Verträglichkeit und Lebensqualität sowie Wechselwirkungen und seltene Nebenwirkungen die Gabe des neuen Präparats weiterhin rechtfertigen.
Aktuelle Studien
Wenn Sie generell Interesse an einer Studienteilnahme haben, können Sie sich gerne bei uns für unsere Proband*innendatenbank registrieren lassen.
Zur Registrierung und wenn Sie Interesse an weiteren Informationen haben, melden Sie sich gerne unter folgender Telefonnummer bei uns: 0228-287-16040 oder Enable JavaScript to view protected content.